Di- und polyfunktionelle Synthesebausteine stellen die Basis zur Herstellung von Kunststoffen dar. In den letzten Jahren rücken hier vermehrt biobasierte funktionelle Moleküle in den Fokus von Forschung und Industrie. Zu den bekanntesten Vertretern dieser biogenen Materialien gehören Kunststoffe auf Basis von Stärke, Zellulose und Polymilchsäure (PLA). Auch Pflanzenöle und Pflanzenölderivate können durch entsprechende Funktionalisierung zu interessanten Monomerbausteinen umgesetzt werden. Das Fraunhofer IGB beschäftigt sich in diesem Forschungssegment mit der biokatalytischen Funktionalisierung von pflanzlichen Ölen oder Fettsäurederivaten zu langkettigen Dicarbonsäuren (lcDCA) oder Pflanzenöl-basierten Epoxiden. Dicarbonsäuren finden beispielsweise Anwendung bei der Herstellung von Polyamiden und Polyestern. Pflanzenöl-basierte Epoxide können als PVC-Stabilisatoren, Weichmacher, zur Synthese von biobasierten Harzen und Beschichtungen oder nach weiterer Umsetzung als Bestandteile von Schmierstoffformulierungen eingesetzt werden.
Bi- und polyfunktionelle Synthesebausteine auf Basis pflanzlicher Öle
Dicarbonsäuren aus Pflanzenölen
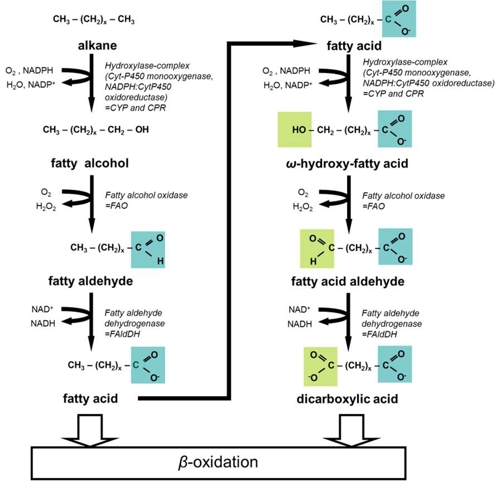
Synthese und Abbau von Dicarbonsäuren
Langkettige Dicarbonsäuren (C > 12) stellen interessante Synthesebausteine zur Herstellung biobasierter Kunststoffe dar und bieten neben ihren ökologischen Vorteilen zusätzlich die Möglichkeit zur Entwicklung neuer Polymere mit speziellen Eigenschaften. Sie sind allerdings chemisch aufwendig zu synthetisieren, können alternativ aber biotechnologisch hergestellt werden. Als Substrat zur mikrobiellen Synthese der lcDCA können beispielsweise Alkane, hydrolysiertes Rapsöl oder Ölsäure von Hefen der Gattung Candida umgesetzt werden.
Die Synthese von langkettigen Dicarbonsäuren in Mikroorganismen erfolgt über die omega-Oxidation, welche für manche Hefen wie z. B. der Gattung Candida oder Yarrowia beschrieben ist. Im Verlauf von drei enzymatischen Reaktionen werden hierbei Fettsäuren zu Dicarbonsäuren oxidiert. Die Mikroorganismen besitzen zudem den biochemischen Abbauweg für Mono- und Dicarbonsäuren, die so genannte beta-Oxidation, welcher in natürlich vorkommenden Hefen die Akkumulation der Dicarbonsäuren verhindert.
Ziele und Strategien: Stamm- und Prozessentwicklung
Am Fraunhofer IGB sollen neue Fermentationsstämme für die Umwandlung von Fettsäuren in Dicarbonsäuren bereitgestellt werden, die aufgrund ihrer Apathogenität einfacher handhabbar sind als der bekannte pathogene Stamm C. tropicalis. Zur Bereitstellung neuer Produktionsstämme werden neu identifizierte Mikroorganismen zum einen als Ganzzell-Katalysatoren in einem integrierten Prozess zur Umsetzung von Fettsäuren eingesetzt, um eine möglichst hohe Dicarbonsäureausbeute zu ermöglichen. Zum anderen werden ausgewählte Stämme gentechnisch modifiziert, um eine Dicarbonsäureakkumulation zu ermöglichen. Auch diese rekombinanten Stämme werden gegenwärtig auf ihre Eignung als Produktionsstämme hin untersucht. Des Weiteren werden die Einsatzmöglichkeiten von Pflanzenölen für die Dicarbonsäureherstellung untersucht, die nicht in Konkurrenz zur Lebensmittelindustrie stehen.
Bisherige Ergebnisse und Ausblick

Durch die Entwicklung unterschiedlicher Fed-Batch-Verfahren mit Mikroorganismen der Gattung Candida konnten bereits Dicarbonsäurekonzentrationen von bis zu 100 g/l aus Ölsäure erreicht werden. Parallel untersuchen wir weitere Mikroorganismen zur Bereitstellung neuer sowie einfacher zu handhabender Produktionsstämme, die eine möglichst hohe Dicarbonsäureausbeute ermöglichen.
Derzeit arbeitet das Fraunhofer IGB an der gentechnischen Modifikation eines Pichia-Stammes. Durch gezielte Deaktivierung (Knock-out) von Genen des beta-Oxidationsweges soll der Abbau der gebildeten Dicarbonsäuren in diesem Stamm verhindert und durch verstärkte Aktivierung von Genen des omega-Oxidationsweges die Dicarbonsäureausbeute gesteigert werden. Dadurch soll ein mikrobiologisch unbedenklicher Produktionsstamm zur Dicarbonsäurebildung zur Verfügung gestellt werden.
Die Verfahrensentwicklung erfolgte am Beispiel von Rapsöl-Derivaten und Ölsäure, kann aller Voraussicht nach aber auf Öle übertragen werden, die nicht im Lebensmittelbereich verwendet werden. In einem zweiten Ansatz werden ausgewählte Stämme gentechnisch modifiziert, um eine Dicarbonsäuresynthese zu gewährleisten. Auch diese rekombinanten Stämme werden gegenwärtig auf ihre Eignung als Produktionsstämme untersucht.
Leistungsspektrum
- Wir bieten Ihnen Fermentationen zur Bereitstellung von Mustern der 1,18-Octadecendisäure, produziert von Candida sp., an.Außerdem bieten wir Ihnen chemisch-enzymatische Modifizierungen von 1,18-DCA, beispielsweise durch Epoxidierung, an.Darüber hinaus verfügen wir über Know-how im Bereich der Stammentwicklung und können auf Ihren Wunsch hin entsprechendes Metabolic Engineering durchführen
Epoxide aus pflanzlichen Ölen
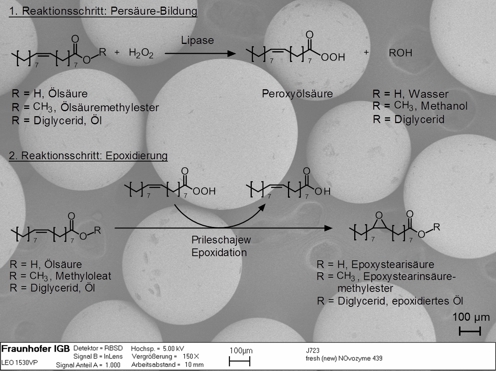
Anwendung und Herstellung pflanzlicher Epoxide
Bei der Epoxidierung ungesättigter Fettsäuren und Triglyzeride entstehen Produkte mit gesteigerter Polarität und Reaktivität. Pflanzenöl-basierte Epoxide werden im industriellen Maßstab meistens ausgehend von Sojaöl chemisch hergestellt. Die Epoxidierung erfolgt dabei über die sogenannte Prileschajew-Reaktion, bei der olefinische Doppelbindungen der ungesättigten Fettsäuren durch Persäure zum Epoxid (Oxiran) umgesetzt werden. Die Persäurebildung erfolgt häufig in situ durch Reaktion von Wasserstoffperoxid mit Essig- oder Ameisensäure unter Verwendung starker Mineralsäuren, beispielsweise Schwefelsäure, oder Ionenaustauschharze als Katalysator. Bei der chemischen Umsetzung sind vor allem die anspruchsvolle Prozessführung aufgrund einer stark exothermen Reaktion, stark saure Reaktionsbedingungen und damit verbundene Nebenreaktionen sowie hohes Salzaufkommen bei der Produktaufarbeitung problematisch.
Eine Alternative zu diesem chemischen Verfahren besteht in der chemo-enzymatischen Epoxidierung, bei der eine Lipase die Persäurebildung aus Fettsäure und Wasserstoffperoxid enzymatisch katalysiert. Wesentliche Vorteile sind mildere Prozessbedingungen und eine höhere Selektivität der Umsetzung. Bei der chemischen Methode auftretende unerwünschte Ringöffnungsreaktionen können beim chemo-enzymatischen Verfahren weitestgehend vermieden werden.
Ziele und Strategien

Das Fraunhofer IGB untersucht in verschiedenen Projekten die oleochemische Nutzung von Ölen und Fetten und befasst sich dabei in einem weiteren Schwerpunkt mit der enzymatischen Herstellung von Epoxidbausteinen für verschiedene Anwendungsgebiete. Der Fokus liegt zum einen auf der Identifikation geeigneter Biokatalysatoren und zum anderen auf der Prozessentwicklung und Skalierung des mehrphasigen Reaktionssystems gemeinsam mit dem Fraunhofer CBP in Leuna. Bei der Auswahl der eingesetzten nachwachsenden Rohstoffe wird besonders Wert darauf gelegt nicht-nahrungsmittelrelevante Substrate zu verwerten.
Bisherige Ergebnisse und Ausblick
Neue Enzyme
In einem Screening konnten am Fraunhofer IGB neue, nicht kommerziell erhältliche Enzyme identifiziert werden, die eine Persäurebildung und somit in einem Folgeschritt eine Epoxidierung ungesättigter Fettsäuren katalysieren. Die Enzyme werden derzeit charakterisiert und auf ihre technischen Einsatzmöglichkeiten hin untersucht. Darüber hinaus könnten eine geeignete Immobilisierung und gegebenenfalls Enzymmodifikationen auf Proteinebene zu einer gesteigerten Aktivität und Stabilität des Biokatalysators beitragen.
Prozessentwicklung
Für die chemo-enzymatische Epoxidierung pflanzlicher Öle und Fettsäuren setzen wir am Fraunhofer IGB hauptsächlich Pflanzenöle ein, welche nicht als Lebensmittel verwendet werden. Wir konnten den Prozess für den Umsatz unterschiedlicher Substrate durch eine immobilisierte Lipase aus Candida antarctica (Novozym® 435) im Hinblick auf Substratkonzentration, Wasserstoffperoxidzugabe, eingesetzter Enzymmenge und Temperatur so optimieren, dass verschiedene ungesättigte Fettsäuren und Öle annähernd vollständig zu den korrespondierenden Epoxiden umgesetzt werden. Im Anschluss an die Verfahrensentwicklung im Labormaßstab soll am Fraunhofer CBP eine Maßstabsvergrößerung erfolgen und Verfahrensschemata für eine Produktionsanlage im technischen Maßstab erstellt und dessen Wirtschaftlichkeit bewertet werden.
Leistungsspektrum
- Wir bieten Ihnen Screening nach geeigneten Enzymen zur Epoxidierung an.
- Außerdem die Bereitstellung biotechnologisch hergestellter Mustermengen an Epoxiden auf Basis verschiedener Pflanzenöle, freier Fettsäuren und Fettsäureestern.
- Zudem bieten wir eine ausführliche Charakterisierung von Pflanzenölepoxiden (Dünnschichtchromatographie, Jodzahl, Epoxidsauerstoffgehalt, FT-IR-Spektroskopie, Rheologie, Dynamische Differenzkalorimetrie, Gaschromatographie) sowie
- Optimierung relevanter Prozessparameter mittels statistischer Versuchsplanung und
- Skalierung bis zum 100-Liter-Maßstab.
 Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB
Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB