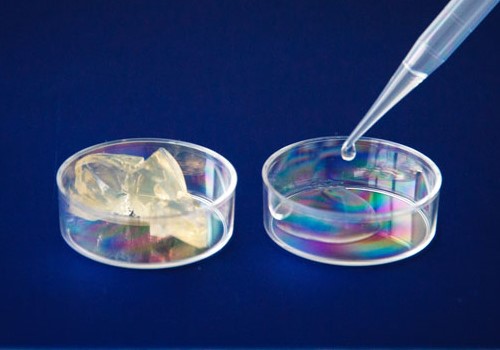
Herausforderung – Regeneration von Gelenkknorpel
Gelenkknorpel hat aufgrund der fehlenden Durchblutung keinen Zugang zu regenerativen Zellpopulationen. Knorpeldefekte sind daher nahezu irreversibel und resultieren häufig in einer fortschreitenden Zerstörung des betroffenen Gelenks. Eine vielversprechende therapeutische Behandlung ist die matrixassoziierte autologe Chondrozytentransplantation (MACT), bei der ein geeignetes Trägermaterial (Matrix) zunächst mit Knorpelzellen (Chondrozyten) des Patienten besiedelt und dann in den Knorpeldefekt implantiert wird. Die Kultivierung der Chondrozyten in den üblicherweise eingesetzten kollagenbasierten Matrices kann jedoch zu einer Dedifferenzierung, das heißt zu einem Funktionsverlust der Zellen führen.
 Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB
Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB